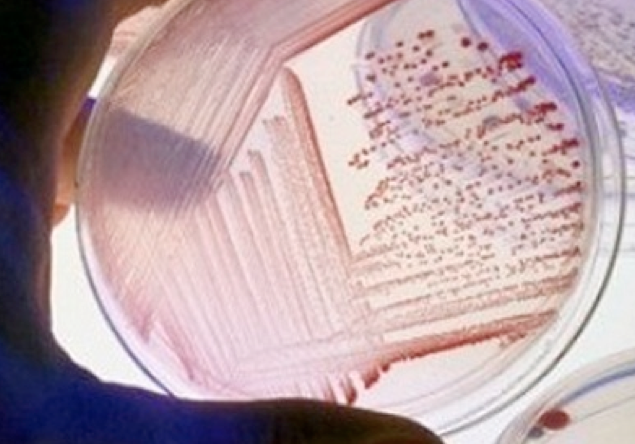
La bactérie E. coli, ou colibacille, très généralement non pathogène (95% des souches ne sont pas dangereuses), est donc un hôte normal, commensal, du tube digestif des mammifères. Anaérobie facultative, longue de 2µm, une seule bactérie peut se multiplier pour théoriquement fournir, en moins de 2 jours, une masse de 6*1021 tonnes, égale à celle de la Terre !
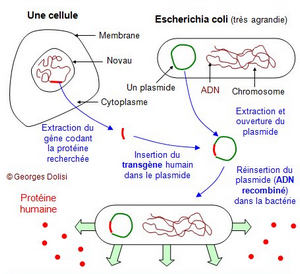
C’est ainsi qu’E. coli produit industriellement, dans des conditions hautement sécurisées, l’hormone hypophysaire de croissance (STH ou hormone somatotrophe), sans les risques de contamination virale comme ceux rencontrés lors de l’utilisation d’hypophyse humaine « naturelle » (décès en France de 117 jeunes traités pour nanisme ; en 2004, la France comptait 58 % des cas mondiaux de maladie de Creutzfeld-Jakob liés à l’hormone de croissance).
L’insuline, les facteurs de coagulation nécessaires aux hémophiles, l’interféron (substance antivirale) ou le vaccin de l’hépatite B sont aussi produits par transgénèse. E. coli permet également de produire des enzymes immobilisées, de servir à la bio-remédiation, etc
La technique de l’ADN recombinant semble permettre la synthèse du ranibizumab, anticorps monoclonal susceptible de se lier et d’inhiber un facteur de croissance (VEGF-A) impliqué dans la dégénérescence maculaire liée à l’âge (1 million de malades en France). Une version « synthétique » de E. coli, créée par James K. Liao à UCLA, lui a permis de faire produire à la bactérie des alcools non naturels à longue chaîne (5 à 8 atomes de carbone), source de biocarburants, compatibles avec le kérosène… La bactérie ne peut cependant pas produire des protéines trop importantes et complexes, contenant des liaisons disulfures multiples, des groupements thiols…
Mais E. coli peut se montrer spontanément ennemie plutôt qu’amie ! Fréquemment impliquées dans un large spectre d’infections à la fois en élevage et en santé humaine (diarrhée, infection urinaire, toxi-infection alimentaire, septicémie, méningite néonatale…), {E. coli est à ce titre une espèce modèle pour étudier le continuum entre bactéries commensales et bactéries pathogènes.
Certaines souches produisent un arsenal de plusieurs dizaines de toxines directement dans les cellules de l’hôte, dont elles piratent les fonctions cellulaires pour coloniser sa muqueuse en échappant à son système de défense.
Ces toxines font partie d’une nouvelle famille, les cyclomodulines : certaines comme la colibactine, non protéique, induit des lésions de l’ADN de l’hôte et pourraient jouer un rôle dans le cancer, d’autres comme la protéine Cif (Cycle Inhibiting Factor) bloquerait la dégradation de protéines clés impliquées dans diverses voies de signalisation cellulaire comme la réponse inflammatoire, la différenciation cellulaire…
E. coli peut devenir pathogène si les défenses de l’homme-hôte se trouvent affaiblies ou si elle acquiert des facteurs de virulence particuliers. Chaque année, une souche de cette bactérie (E. coli entéro-toxique ou ETEC) infecte quelques 200 millions de personnes et entraîne le décès de près de 400 000 d’entre elles, la plupart dans les pays en développement, mais pas uniquement. En effet, une série d’intoxications alimentaires sévères ont été observées depuis les années 1980, notamment aux Etats-Unis (250 décès en 1996). Appelée « maladie du hamburger », elle est due à une souche 0157:H17, désormais très étudiée, à l’origine de diarrhées hémorragiques, voire du Syndrome Hémolytique et Urémique (SHU), dont l’issue peut être fatale. La contamination se fait par de la viande, notamment de bœuf, insuffisamment cuite, des produits laitiers non pasteurisés et d’autres produits solides ou liquides ayant été en contact avec l’agent infectieux ou simplement par contact avec les animaux porteurs.
La classification des variants de bactéries (et de virus, de cellules…), le sérotypage, principe découvert par la microbiologiste américaine Rebecca Lancefield en 1933, est basé sur une variété de facteurs, incluant la virulence (mesure quantitative du pouvoir pathogène), la présence ou non de toxines et leur nature, les plasmides, etc. permettant de différencier 2 éléments d’une même espèce. L’antigène somatique O, définissant le sérogroupe, est contenu dans les lipopolysaccharides présents sur la paroi bactérienne des souches à Gram négatif. L’antigène flagellaire H est de nature protéique et entre dans la structure du flagelle (cilliature péritriche) permettant la mobilité de la bactérie. L’antigène K de surface n’est pas toujours présent mais s’il est présent, il bloque l’agglutinabilité de l’antigène O.
La rapidité de multiplication de E. coli fait que l’ingestion d’une dose infectieuse très faible (inférieure à 100 unités formant colonies) peut induire, après une incubation de quelques jours, des infections dont les tableaux cliniques sont variés : de la diarrhée bénigne à la colite hémorragique, qui peut se compliquer, au bout de plusieurs jours en SHU ou plus rarement en purpura thrombotique et thrombocytopénique (PTT), selon le système vasculaire le plus atteint par les lésions induites par la toxine, le rein pour le SHU, le système nerveux pour les PTT. Les {E. coli sont également pathogènes dans des localisations extra-intestinales, à l’origine de méningites, d’abcès, de péritonites, de septicémies et surtout d’infections urinaires (UPEC).
Les toxines incriminées, appelées shigatoxines ou Stx, sont des holoprotéines, c’est-à-dire qu’elles sont uniquement constituées d’oligomères d’α-aminoacides, d’environ 70 kDa. Un mécanisme complexe, mais assez bien élucidé sur certains modèles animaux sensibles, montrent l’activation d’une réponse inflammatoire et le développement de lésions au niveau de la barrière intestinale, favorisant ainsi la dissémination systémique de la toxine au niveau de l’organisme.
L’absence de récepteur pour les toxines Stx expliquerait que les ruminants ne développent pas l’infection, mais en soient des agents passifs, via notamment leurs déjections.
Il existe une très grande variabilité dans les protéines des différentes souches pathogènes : les gènes codant pour les principaux facteurs de virulence sont portés par des éléments mobiles du génome, éléments acquis lors[ d’échanges génétiques. C’est le cas pour la nouvelle souche en cause dans l’épidémie actuelle d’E. coli entéro-hémorragique qui a été caractérisée. Le séquençage de son génome, réalisé au Beijing Genomics Institute, en Chine, a révélé que c’est une « nouvelle souche hyper-toxique », un hybride, O104:H4 produisant des Stx, qui a acquis une partie de sa virulence de souches entéro-agrégatives d’E. coli (EAEC), par transfert horizontal de gènes.
Dans le cas de l’épidémie allemande, et d’une partie au moins de l’épidémie bordelaise, diverses graines en seraient les agents passifs, les vecteurs : les graines, même très légèrement contaminées, mises à germer dans une atmosphère humide et chaude, deviennent alors de véritables bouillons de culture…
Il n’existe pas de traitement efficace actuellement. Que révèle « l’affaire de la bactérie tueuse » ? Qu’il vaut mieux une intoxication alimentaire par du bio que par un additif chimique ? Quant au coût socio-économique de l’emballement médiatique, on est loin de le connaître !
Pensée du jour
«Concombre mortel, produits chimiques toxiques… et pourtant, nous continuons à gagner 3 mois d’espérance de vie par an ! Bizarre, vous avez dit bizarre ?»
Sources
– http://fr.wikipedia.org/wiki/Escherichia_coli
– http://georges.dolisi.free.fr/Microbio/Genie_gen.htm
– http://fr.wikipedia.org/wiki/Hormone_de_croissance
– http://en.wikipedia.org/wiki/Escherichia_coli_(molecular_biology)
– http://en.wikipedia.org/wiki/Ranibizumab
– http://www.pnas.org/content/early/2008/12/08/0807157106.abstract
– http://www.inra.fr/les_recherches/exemples_de_recherche/bacteries_genotoxiques_tube_digestif
– Pathogenic bacteria target NEDD8-conjugated cullins to hijack host-cell signaling pathways.
PLoS pathogens, 2010
– http://fr.wikipedia.org/wiki/Syndrome_hémolytique_et_urémique
– http://www.facmv.ulg.ac.be/amv/articles/2007_151_4_02.pdf
– A. Chaded, B. China, G. Daube, {Ann. Méd. Vét. 2007, 151, 215-246
– http://fr.wikipedia.org/wiki/Escherichia_coli_O104:H4
– http://fr.wikipedia.org/wiki/Épidémie_de_syndrome_hémolytique_et_urémique_de_2011

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie