Le Vanadium, symbole V, Numéro atomique 23 Est un métal pas très abondant, blanc argenté, De masse atomique 50,9 et de densité d = 6.
Il est de structure cubique centrée, il s’oxyde au delà de 900° mais il est très stable à température ordinaire. Il fait partie des métaux de transition
Le vanadium est présent dans de nombreux minerais tels que la vanadinite qui est un chlorovanadate de plomb (Pb5VO4Cl), la carnotite qui est un vanadate double d’uranyle et de potassium. Il se trouve aussi dans les minerais de titane, ce qui amène en aval des usines de fabrication d’oxyde de titane des eaux chargées en vanadium qui enrichissent les fleuves et estuaires (la Seine par exemple) en sels de ce métal. Les hydrocarbures, le pétrole et le charbon contiennent en général de l’ordre de 50 mg de vanadium par kilogramme. Leur combustion dégage ainsi près de 10 à 30 000 t de vanadium dans l’atmosphère sous forme d’oxydes, ce qui constitue une source anthropique majeure de pollution. Toutefois, à faible dose dans l’organisme, le vanadium est un oligoélément nécessaire à la vie.
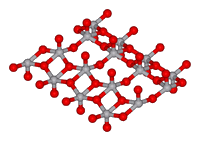
L’oxyde VO2, noir bleuté, a la même structure que l’oxyde de titane, mais un changement de structure cristalline à 65°C le fait passer de l’état isolant à l’état conducteur électrique de façon très spectaculaire.
Le Vanadium est un composant d’alliages très important. On l’ajoute aux aciers sous forme de ferro-vanadium pour donner des aciers spéciaux tels que les aciers inoxydables durs et résistants pour les couteaux ou les instruments chirurgicaux. Allié au fer et au chrome il donne les aciers chrome-vanadium très utilisés pour l’outillage. Enfin les alliages avec le titane, par exemple le TAV6 (90 % de titane, 6 % d’aluminium et 4 % de vanadium), présentent le meilleur rapport robustesse/légèreté et sont essentiels en construction aéronautique ou spatiale. Ces utilisations de haute technologie en font un métal coûteux autour de 36 €/kg et quasi stratégique, avec seulement quelques compagnies productrices et trois grands pays qui se partagent l’essentiel d’un marché de quelques 60 000 t/an : l’Afrique du Sud, la Chine et la Russie.
Ainsi la pensée chimique du jour ne peut-être que :
« Préférez une clé en chrome-vanadium plutôt qu’une clé au bras »
Sources :
– http://fr.wikipedia.org/wiki/Vanadium
– http://en.wikipedia.org/wiki/Vanadium

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie