Vers une chimie douce bio-inspirée

Vers une chimie douce bio-inspirée
Depuis des millénaires, les verres et les céramiques sont fabriqués en chauffant le sable ou l’argile dans des fours à très haute température. Pourtant, l’observation du vivant nous montre que certains micro-organismes ont appris à développer des conditions de synthèse beaucoup plus douces, compatibles avec la vie. De simples micro-algues, comme les diatomées, élaborent ainsi leurs coques de silice. La nature peut-elle nous inspirer pour fabriquer des verres dans des conditions plus douces ?
Biomimétisme et bio-inspiration : quand la nature inspire le chimiste !
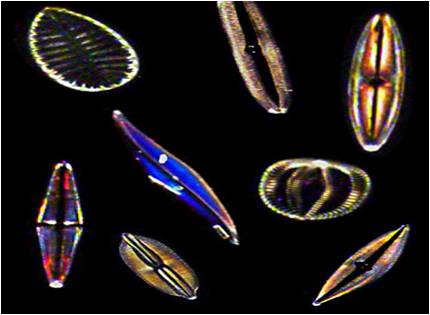
Les diatomées sont des algues unicellulaires microscopiques, photosynthétiques, qui se trouvent en abondance dans le plancton, les lacs et les rivières. Elles y jouent un rôle écologique primordial puisque par photosynthèse, elles consomment plus du quart du CO2 que nous relâchons dans l’atmosphère.
Elles synthétisent leur squelette de verre à basse température à partir de silice dissoute dans l’eau. Cette carapace, appelée frustule, est de l’ordre de quelques dizaines de microns (μm), elle les protège du milieu extérieur mais sa porosité permet les échanges avec le milieu extérieur.

Le verre est classiquement fabriqué à partir de la silice SiO2 par fusion à 1 500 °C. Le verre en fusion peut être moulé, soufflé ou filé par extrusion. Les filaments sont ensuite séchés à 700-800 °C pour obtenir des fibres.
Contrairement à nos verriers, les diatomées réalisent la synthèse du verre à température ambiante, et elles le font depuis des millions d’années !
Si on peut obtenir du verre par chimie douce, non seulement on a un gain d’énergie mais surtout on crée des matériaux hybrides organiques/inorganiques qui allient des propriétés inorganiques (résistance mécanique, résistance aux UV…) et les fonctionnalités organiques (comme la couleur, la luminescence…). Par exemple colorer du verre avec des molécules organiques devient possible en chimie douce alors que c’est impossible avec le procédé de fabrication du verre traditionnel car la matière organique brûle à 1 500 °C.
La nature pourrait-elle devenir une source d’inspiration pour élaborer les matériaux du futur ?
Trouve les applications industrielles inspirés par la nature !
Les diatomées : des nanomatériaux vivants !
Les diatomées nous offrent un superbe exemple de ce que le vivant sait faire dans le domaine des matériaux nanostructurés. Ces protistes s’entourent d’un exosquelette de silice poreuse (frustule) qui les protège, tout en laissant passer la lumière du Soleil. Après leur mort, les diatomées se déposent au fond des océans, où les frustules de silice donnent naissance à une roche sédimentaire connue sous le nom de « terre de diatomées » ou « diatomite » [2].
Par érosion des sols, la silice se dissout légèrement dans l’eau et donne des espèces dissoutes : l’acide silicique, à partir de laquelle les diatomées élaborent leur carapace de silice :
SiO2 + 2 H2O → Si(OH)4
La construction d’un réseau de silice met en jeu des réactions de polycondensation au cours desquelles l’élimination d’une molécule d’eau entre deux groupements hydroxyle conduit à la formation d’un oxygène pontant :
(HO)3Si-OH + HO-Si(OH)3 → (HO)3Si-O-Si(OH)3 + H2O
La réaction complète conduit à la silice : Si(OH)4 → SiO2 + 2H2O
La synthèse de silice par précipitation en milieu aqueux est difficile à contrôler. C’est pourquoi les chimistes utilisent des précurseurs moléculaires, les alcoxydes Si(OR)4, tels que le TMOS (tétraméthoxysilane, R = CH3) ou le TEOS (tétraéthoxysilane, R = C2H5). Ils réalisent le procédé « sol-gel » (solution-gélification) en milieu acide, en deux étapes :
– l’hydrolyse des précurseurs alcoxydes en solution conduit à la substitution des groupes alcoxyle (-OR) par des groupes hydroxyle (-OH). La solution de Si(OH)4 ainsi obtenue est appelée « SOL » ;
– par condensation, les molécules de Si(OH)4 se lient entre elles par des ponts oxo (-O-), avec élimination d’eau. La condensation se poursuit dans toutes les directions et forme un « GEL » de silice SiO2.
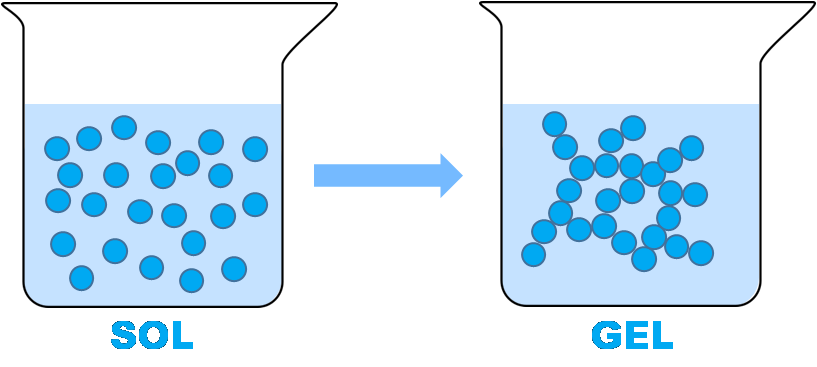
La silice est ainsi obtenue à partir de précurseurs moléculaires en solution (acide silicique ou alcoxydes) par des réactions de polymérisation inorganique analogues à celles que l’on utilise pour synthétiser les polymères organiques.
Ce gel contient encore du solvant. Il faut procéder au séchage. Si on laisse le gel vieillir naturellement, le phénomène de réticulation conduit au rétrécissement du matériau avec expulsion du solvant : on parle alors de « synérèse » (du grec sun, « avec », et airein, « prendre » (cf. aphérèse, diérèse).
À partir d’une même solution et en fonction du mode de séchage du gel, le matériau final prend des formes très différentes : fibres, films et couches minces, avec un séchage conventionnel on obtient des poudres, avec un séchage lent suivi d’un frittage on obtient des matériaux denses ou massifs comme des monolithes de verres ou des céramiques, avec un séchage supercritique on obtient des aérogels.
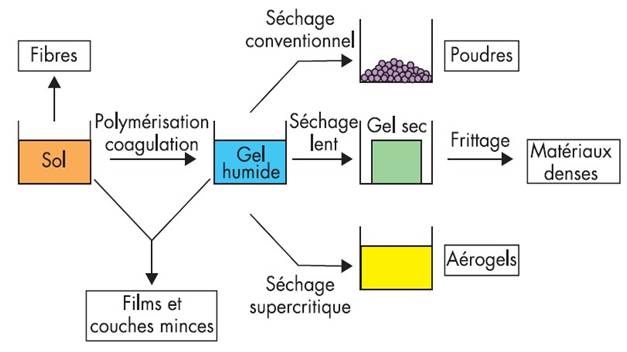
En plus d’un gain d’énergie évident, le procédé sol-gel, basé sur des réactions chimiques, permet de contrôler le déroulement de la réaction à chaque étape de la synthèse, depuis le précurseur moléculaire jusqu’au solide final.
On peut ainsi élaborer des « matériaux sur mesure » dont la composition, la structure et même la morphologie sont optimisées en fonction de l’application désirée. Pour l’industriel, l’avantage principal réside dans la possibilité de mettre en forme le matériau directement à partir de la solution sans passer par des poudres comme il est d’usage dans l’industrie du verre ou de la céramique. Le produit obtenu, un gel de silice hydratée (SiO2, nH2O), ne permet pas d’élaborer un verre massif car l’élimination de l’eau contenue dans le gel conduit généralement à une poudre.
De nombreuses méthodes de dépôt ont été mises au point (dip-coating, spin-coating, pulvérisation…). Elles sont maintenant développées commercialement par de nombreux verriers pour valoriser les vitrages utilisés dans le bâtiment ou l’automobile. Les particules de silice colloïdale, de dimensions contrôlées, ont été commercialisées sous le nom de silice Stöber. L’extrusion des gels permet de réaliser des fibres de silice ou d’alumine directement sans passer par la fusion de ces oxydes réfractaires. C’est ainsi que les tuiles réfractaires de la navette spatiale Columbia ont été élaborées à partir de fibres céramiques sol-gel.
Les procédés sol-gel ne permettent pas seulement de développer des méthodes d’élaboration originales ; ils permettent aussi, et surtout, de synthétiser des matériaux nouveaux impossibles à obtenir par les voies classiques, comme les hybrides organominéraux. Les conditions de chimie douce mises en jeu lors de l’élaboration de verres ou de céramiques par voie sol-gel sont très semblables à celles de la chimie organique. Il est donc possible de mélanger des espèces organiques et minérales au sein d’une même solution pour former des matériaux hybrides, véritables nanocomposites à l’échelle moléculaire.


On obtient ainsi toute une gamme de nouveaux matériaux allant du verre fragile au polymère plastique. Cette chimie des matériaux hybrides connaît aujourd’hui un développement exponentiel. Elle rassemble les chimistes du solide, des solutions, des polymères et des molécules organiques. Les applications industrielles des hybrides organominéraux sont très nombreuses : depuis la simple semelle d’un fer à repasser jusqu’au toit du grand théâtre national de Pékin. Ce dôme de verre est recouvert d’un film sol-gel autonettoyant, constitué de nanoparticules d’oxyde de titane TiO2 dispersées dans une matrice hydrophile.
Un domaine particulièrement développé concerne l’optique sol-gel, dans laquelle des molécules organiques optiquement actives sont dispersées dans une matrice minérale qui assure transparence, propriétés mécaniques et protection.
Chimie douce et biotechnologie
1. Des enzymes immobilisées
Les biotechnologies mettent à profit les propriétés catalytiques des enzymes. Ces enzymes sont immobilisées sur des supports solides de façon à pouvoir les recycler après utilisation. Les matériaux utilisés actuellement sont essentiellement des polymères organiques ou biologiques. Ils présentent l’avantage d’être biocompatibles mais leurs propriétés mécaniques ne sont pas très bonnes et ils gonflent souvent en présence d’eau, laissant ainsi s’échapper les molécules actives.
Les procédés sol-gel, qui s’effectuent dans des conditions particulièrement douces, offrent de nouvelles possibilités pour l’encapsulation d’espèces biologiques. L’encapsulation se fait simplement en mélangeant les enzymes avec une solution de précurseurs. La silice condense autour des enzymes qu’elle enveloppe comme une cage. L’enzyme se trouve ainsi emprisonnée au sein d’une matrice de silice qui la protège, qui ne gonfle pas et dont la porosité peut être rigoureusement contrôlée. L’enzyme conserve son activité catalytique et sa durée de vie peut être multipliée par un facteur cent.
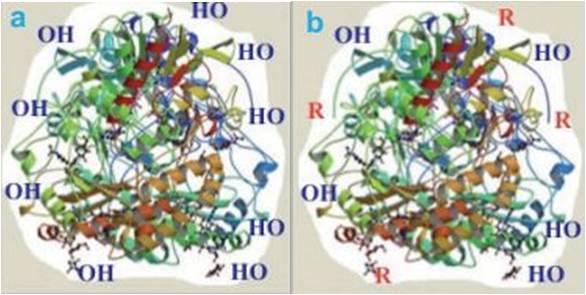
On peut même contrôler la nature chimique de la matrice hybride qui entoure l’enzyme de façon à optimiser ses propriétés. Des résultats remarquables ont été obtenus avec les lipases. Ces enzymes, qui catalysent les réactions d’hydrolyse-estérification, jouent un rôle important dans l’industrie agroalimentaire, le pétrole et la synthèse organique.
Elles agissent en général dans des émulsions, à l’interface entre les phases hydrophile et hydrophobe. Un processus d’activation interfaciale se produit alors, qui modifie l’accessibilité du site actif de l’enzyme. Fermé par une chaîne peptidique en milieu hydrophile, il s’ouvre en milieu apolaire. Piégées dans une matrice de silice hydrophile, les lipases sont relativement peu actives, mais on peut accroître considérablement leur activité en contrôlant la balance hydrophile-hydrophobe de la matrice hybride au sein de laquelle elles sont piégées.
De telles enzymes sol-gel sont maintenant commercialisées. Elles offrent des performances bien supérieures à celles des lipases classiques.
2. Des cellules vivantes dans une cage de verre !
Les diatomées sont des protistes dans lesquels une cellule vivante est enfermée dans une carapace de silice. Peut-on imiter la nature en piégeant des cellules vivantes au sein d’une cage de verre ?
De nombreux micro-organismes tels que des bactéries, des champignons, des micro-algues, des cellules végétales et même des cellules animales ont été immobilisés au sein de gels de silice. Les études réalisées montrent que ces cellules conservent leur activité métabolique pendant plusieurs semaines, voire même plusieurs mois. Comme les enzymes, les cellules immobilisées peuvent servir de biocapteurs. C’est ainsi que des bactéries recombinantes ont été immobilisées dans un film de silice transparente. Génétiquement modifiées de façon à exprimer des protéines (GFP) qui deviennent luminescentes en présence de certains agents chimiques ou biologiques, elles permettent de réaliser des biocapteurs remarquablement spécifiques et sensibles. On peut contrôler la porosité de l’enveloppe de silice qui entoure les cellules de façon à réguler ses échanges avec le milieu extérieur.
Des réactions de reconnaissance spécifique antigène-anticorps ont été effectuées au sein de gels de silice. On a pu ainsi réaliser des capteurs extrêmement sensibles permettant de détecter des traces de polluants tels que l’atrazine ou d’explosifs comme le TNT.
Avec l’aide du service de parasitologie de la Pitié-Salpêtrière, ces essais ont été étendus au domaine biomédical en réalisant des tests immunologiques utilisant des cellules d’un parasite (Leishmanie) comme matériel antigénique. Piégées dans un gel de silice, elles conservent la propriété de fixer les anticorps présents dans le sérum d’un patient atteint de leishmaniose.
On peut ainsi réaliser des tests sanguins dans des conditions particulièrement simples. Les résultats obtenus dépendent directement de la porosité du gel. La taille des pores doit être suffisante pour laisser passer les anticorps tout en retenant les cellules. Dans d’autre cas par contre, il faut créer une barrière qui s’oppose au passage des anticorps.
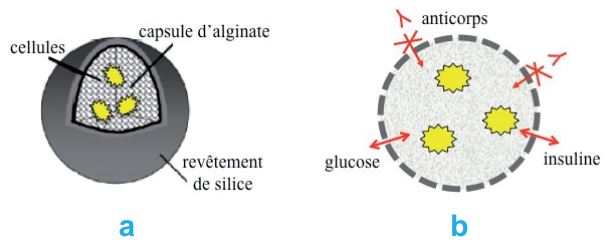
Des études particulièrement spectaculaires ont été réalisées en Italie dans le domaine de la transplantation d’îlots de Langerhans. Ces cellules du pancréas interviennent dans le métabolisme du glucose et la production d’insuline ; leur déficience entraîne le diabète. Les îlots issus d’un organisme sain ont été immobilisés dans des capsules de silice. Les expériences de transplantation réalisées in vivo sur des souris, ou par dérivation de la veine porte dans le cas de patients humains, ont montré que les cellules encapsulées conservaient leur activité métabolique et que de plus, elles étaient protégées du rejet immunitaire par la couche de silice nanoporeuse qui ne permettait pas aux anticorps d’atteindre leur cible.
3. Vers des matériaux vivants !
Des micro-organismes tels que des levures, des bactéries ou des micro-algues sont fréquemment utilisés en biotechnologie pour produire des substances actives. Les produits de leur métabolisme trouvent de nombreuses applications en pharmacie, cosmétique ou alimentation. Il est donc tentant d’utiliser les gels de silice pour réaliser des bioréacteurs. Pour la production de molécules actives, l’astaxanthine, un antioxydant puissant pouvant être utilisé comme complément alimentaire, peut être produit au sein d’un gel de silice par l’algue Haematococcus pluvialis. Le produit actif est extrait à l’aide d’un solvant tandis que les micro-algues encapsulées sont remises en culture de façon à assurer une bioproduction en continu.
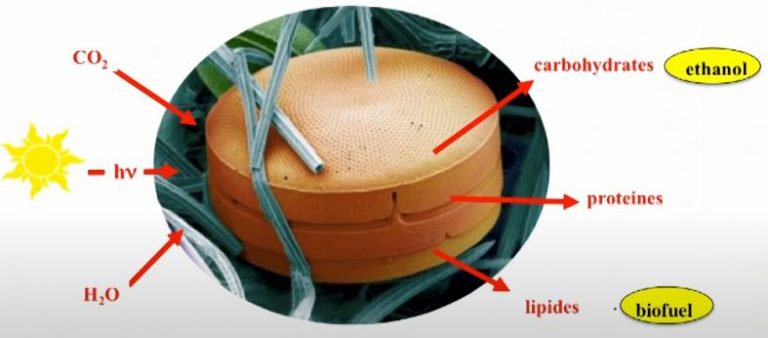
Dans le cadre du réchauffement climatique lié au gaz carbonique, des recherches sont actuellement effectuées afin de fixer le CO2 en excès par photosynthèse. Des résultats particulièrement intéressants ont été obtenus récemment avec des micro-algues photosynthétiques et des cellules végétales immobilisées au sein de gels de silice hybride. Le système imite le comportement photosynthétique des végétaux. Il utilise la lumière solaire pour convertir l’eau en dioxygène et le CO2 en composés organiques à température et pression ambiantes.
Les cellules encapsulées conservent leur activité pendant plusieurs mois. Elles peuvent être recyclées, mais faute de place, elles ne peuvent pas se diviser au sein du gel, ce qui limite l’intérêt du photobioréacteur. Cet inconvénient a pu être évité en immobilisant les cellules au sein de capsules d’alginate autour desquelles on fait condenser un gel de silice. L’alginate est ensuite dissous, laissant des cavités au sein desquelles les cellules peuvent se diviser. On réalise ainsi des bioréacteurs dans lesquels la matrice de silice joue à la fois un rôle de protection et de filtre.
4. Des vecteurs thérapeutiques pour la nanomédecine
Les nanoparticules de silice poreuse ou mésoporeuse trouvent actuellement des applications intéressantes en nanomédecine.
De nombreuses méthodes (voie aérosol, microémulsions…) permettent de synthétiser des particules d’une centaine de nanomètres de diamètre, suffisamment petites pour traverser les parois cellulaires. Des molécules cibles peuvent être greffées à leur surface via des agents de couplage. On peut ainsi conférer à ces nanoparticules des propriétés de furtivité et de ciblage qui leur permettent de se concentrer spécifiquement sur les cellules cancéreuses.
De telles particules, dopées avec des fluorophores, ont été développées en imagerie médicale pour détecter la présence de tumeurs ou en photothérapie dynamique pour les détruire. Dans ce dernier cas, on introduit un photosensibilisateur qui, activé sous l’effet d’une irradiation externe, provoque la destruction des tissus qui l’entourent.
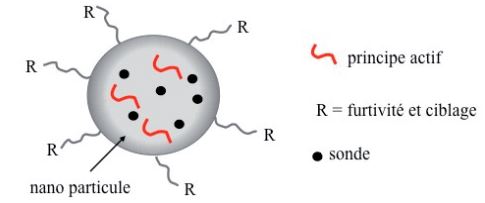
Ces nanoparticules peuvent aussi être utilisées comme vecteurs pour transporter des médicaments au sein des tumeurs et les libérer in situ de façon contrôlée. Elles permettent de diminuer la toxicité des agents thérapeutiques et d’accroître leur efficacité en les délivrant au sein même des cellules malades tout en épargnant les autres cellules saines.
De nombreux médicaments anticancéreux tels que la campothécine sont hydrophobes et donc non solubles dans l’eau ; il est par conséquent difficile de les administrer directement. On peut alors les immobiliser au sein de nanocapsules de silice mésoporeuse qui permettent de les transporter jusqu’à la tumeur.
Conclusion
L’observation de la nature peut servir de source d’inspiration pour imaginer des matériaux qui n’existaient pas auparavant !

D’après l’article de Jacques Livage paru dans L’Actualité Chimique, n° 348-349, janvier-février 2011, p. 64.
Jacques Livage, professeur honoraire au Collège de France, membre de l’Académie des sciences.
Enrichissez vos connaissances !
Quiz

Les procédés sol-gel ont de passionnantes histoires à nous raconter !
Etymologie sur les procédés sol-gel
Procédé sol-gel… Ces mots peuvent prendre plusieurs sens. Ici, sol est l’abréviation de solution et un sol est une solution colloïdale, alors que gel est l’abréviation de gélification et un gel est un milieu semi-liquide figé.
Dans un procédé sol-gel, le milieu passe successivement par les états, de sol et de gel. Si le mot sol, ou solution, vient directement du latin solutio, du verbe solvere, « dissoudre », le mot gel, ou gélification, vient aussi, mais indirectement, du latin.
Les mots latins gelu, gelare signifient « gel », « geler », au sens du froid et de la solidification par le froid, sens conservé en italien, gelare (d’où gelato, « crème glacée ») et en français, geler.
C’est en italien au XIIIe siècle qu’est attesté gelatina, pour désigner le milieu semi-liquide figé car il ressemble à un milieu aqueux solidifié par le froid. De là vient en français la gélatine, une gelée (de fruits), puis gelatin(e), jelly en anglais, sans rapport avec to freeze, « geler », et frost, « gel », s’agissant du froid. Enfin au XIXe siècle, sont apparus en anglais les termes gel, abréviation de gelatine, gelling repris en français, gel (de silice par exemple), gélification.
Cultivez vos jardins chimiques
La croissance de la frustule de la diatomée peut être illustrée par les jardins chimiques : c’est parti !
Protocole
– placer une solution de silicate (SiO44-) de sodium dans un bécher ;
– déposer délicatement de la poudre de sel métallique (sels de fer, cobalt, nickel, calcium…) au fond de la solution à l’aide de « pailles spatules » ;
– observer. La polymérisation se fait et on voit croître la silice ;
Au départ on a une solution d’ions silicates. En ajoutant le cation métallique on provoque la condensation autour du cation.
Explication
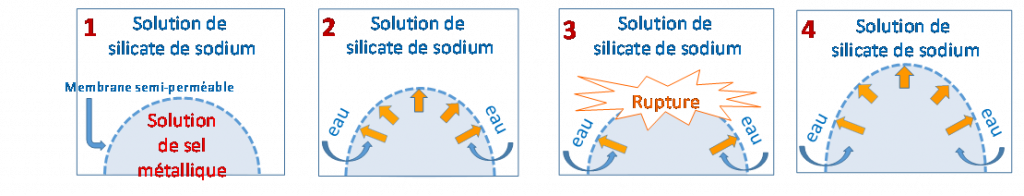
1 – La dissolution des sels métalliques entraîne l’acidification du milieu. Cette variation de pH (diminution) provoque la condensation des ions silicates avec formation d’une membrane en verre, poreuse.
2 – La membrane semi-perméable formée, sépare deux solutions de concentrations en cations différentes. L’eau présente dans la solution de silicate traverse la membrane sous l’effet du phénomène d’osmose, il y a passage de molécules d’eau de l’extérieur de la membrane vers l’intérieur. L’osmose est le passage de molécules de solvant d’une solution A moins concentrée vers une solution B plus concentrée, à travers une membrane semi-perméable (perméable aux molécules de solvant et non perméables aux molécules de soluté). Ce passage crée une pression osmotique.
3 – La pression augmente à l’intérieur de la membrane, la membrane casse.
4 – La membrane se reforme et ainsi de suite…
Philippe Belleville, directeur de recherche au Laboratoire Sol-Gel et Simulation du CEA, nous parle de la chimie sol-gel et de ses applications
Réadaptation de l'article et contenus pédagogiques
Minh-Thu Dinh-Audouin, journaliste scientifique à L’Actualité Chimique.
Myriam Dubreuil, professeure de physique chimie au lycée Déodat de Séverac (Toulouse).
Notes et références
[1] La diatomite est utilisée couramment pour filtrer l’eau des piscines ou les liquides alimentaires tels que le vin, comme support de catalyseur, ou encore comme charge dans les plastiques. La production de diatomite en France est de l’ordre de 200 000 tonnes par an.
[2] Voir la conférence de Jacques Livage, La chimie douce quand la nature inspire la science, et la conférence de Clément Sanchez, La nature, source d’inspiration.
[3] Vidéo sur Les métiers au laboratoire Chimie sol-gel et simulation au CEA.

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie