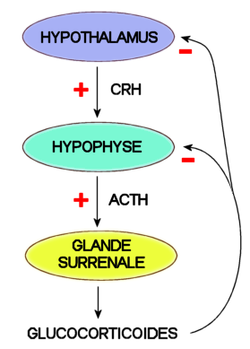
L’ACTH est un petit peptide de 39 acides aminés secrété dans l’hypophyse. Son précurseur est un polypeptide, le gène POMC (pro-opiomélanocortine). En se fixant sur des récepteurs membranaires de la glande corticosurrénale, le gène POMC entraîne une augmentation de la concentration intracellulaire en AMPc, suivie d’une activation des protéines kinases responsables de la transformation du cholestérol en prégnénolone, précurseur commun des corticoïdes. Le gène POMC est également responsable de la synthèse des β-endomorphines (cf. Morphine, Chocolat) et des mélanotropines (ou MSH) à l’origine de la pigmentation de la peau. L’ACTH est produite en excès lors d’un stress.
Les glucocorticoïdes, dont les principaux représentants naturels sont le cortisol (ou hydrocortisone) et la corticostérone, ne possèdent pas de résidu glycosidique. Leur dénomination vient de ce que le cortisol intervient dans la néoglucogénèse entraînant une augmentation de la glycémie, taux de sucre dans le sang. Il intervient aussi dans la régulation du métabolisme des graisses, des protéines et des glucides. Le stress qui provoque leur libération dans le cortex des glandes surrénales peut être autant psychique que métabolique et dans les deux cas, la libération de glucose donne à l’organisme stressé les moyens énergétiques de faire face.
Les glucocorticoïdes ont la particularité, comme la mélatonine, d’être synthétisées sur un rythme circadien (période de 24 h), entre 2 h et 8 h du matin (pic qualifié d’acrophase), induit par une hormone peptidique (Crh) hypothalamique. La cortilosémie (concentration du cortisol circulant) est minimale le soir (bathyphase) avant le sommeil. La libération du glucose à partir du glycogène hépatique et musculaire suit le rythme circadien, car les besoins sont plus importants au début de la journée. Une périodicité annuelle a également été observée, avec une production plus importante en été qu’en hiver. Une corrélation a été établie entre ces rythmes et les performances sportives. Chez les patients schizophrènes, insomniaques ou déprimés, l’administration de mélatonine en soirée peut compenser la production précoce de cortisol avec des effets significatifs sur le comportement.
Le cortisol et la corticostérone sont les hormones actives chez l’homme, la cortisone, qui peut être réduite en cortisol, est inactive en tant qu’hormone. Le récepteur des glucocorticoïdes actifs se fixe sur l’ADN (cf. ADN), provoquant l’expression de gènes-cibles (ou trans-activation), ce qui conditionne la plupart de leurs effets secondaires métaboliques et cardiovasculaires. Le phénomène inverse, appelé trans-répression, est également possible, empêchant la transcription de gènes immunes comme celui codant pour l’interleukine-2.
L’exposition des organismes aux polluants organiques persistants (les POPs) entraînerait une production de cortisol, dommageable chez le fœtus. En 2002, 42 % des substances mises en évidence en France lors des contrôles antidopages étaient des glucocorticoïdes (26,4 % chez les cyclistes).

Un effet important du cortisol est son action anti-inflammatoire ; le cortisol et de nombreux dérivés synthétiques apparentés ont donc été utilisés dans ce but, avec des effets secondaires parfois sévères, comme la suppression de l’immunité par trans-répression, la fonte musculaire, la redistribution des graisses (pas toujours souhaitable !), la perte de neurones (avec les effets sur la cognition, la mémoire, etc.) et jusqu’à la mort de cellules (apoptose), la dépression nerveuse et même la cataracte. Plusieurs de ces phénomènes apparaissent « naturellement » au cours du vieillissement, et la diminution significative de la concentration en cortisol dans le liquide céphalo-rachidien des personnes âgées conforte l’idée qu’il y a bien une relation de cause à effet.
Le cortisol peut avoir une action « minéralocorticoïde » forte, lorsqu’il est utilisé à des doses thérapeutiques élevées et entraîner une forte rétention d’eau. Il en va de même de la cortisone utilisée comme anti-inflammatoire, produite dans le rein à partir du cortisol par l’oxydation en présence de NAD+. Dans le foie, le cerveau, le muscle et d’autres tissus, une 11β-hydroxystéroïde déshydrogénase utilise le NADPH comme cofacteur pour réduire la cortisone en cortisol. Les effets anti-inflammatoires sont liés à la diminution de la production de prostaglandines et de leucotriènes, de sérotonine (cf. Prozac) et d’histamine.
Lorsque l’on parle de « cortisone » en traumatologie, orthopédie, et rhumatologie, et en particulier d’infiltration dans le cas de blessures, tendinites, etc., il ne s’agit pas nécessairement du composé chimiquement défini, mais souvent de corticoïde(s). Les effets bénéfiques de la cortisone, observés depuis les premières infiltrations (1951) sont indéniables : réduction de la réaction inflammatoire et augmentation de la concentration d’acide hyaluronique dans le liquide synovial (cf. GAGs I, GAGs II).
L’utilisation de cortisone sous forme de comprimés, de spray, de solution injectable a soulagé de nombreux patients. Après un traumatisme crânien on peut, momentanément, administrer de la cortisone à forte dose de manière à diminuer rapidement l’œdème intracrânien et ainsi préserver l’intégrité des neurones, voire sauver la vie du patient. On l’utilise également dans le cas d’allergie, d’asthme, dans le traitement des greffes, les poussées de sclérose en plaque…; elle peut être administrée pendant la grossesse, et dès la petite enfance en cas de polyarthrite. Mais la cortisone peut entraîner, sur le long terme, une série d’effets négatifs : une ostéoporose, des tassements de vertèbres, la fonte des muscles ou encore des troubles psychologiques.
Les minéralocorticoïdes tirent leur nom de leur action sur la rétention de l’ion sodium. L’aldostérone est le principal minéralocorticoïde endogène chez l’homme. La corticostérone en est le précurseur, via la désoxycorticostérone ou DOC. Ils se différencient des glucocorticoïdes par l’existence d’un récepteur spécifique. La cortisone formée dans le rein ne se lie pas à ce récepteur et seule l’activité de l’aldostérone est observée. Elle régule la pression artérielle en favorisant l’élimination urinaire des ions potassium et la rétention rénale des ions sodium.
L’aldostérone agit aussi sur les cellules endothéliales des vaisseaux sanguins (régulation de la pression sanguine), sur le cœur (fibrose cardiaque), au niveau du système nerveux central et sur les glandes sudoripares. Sa synthèse dans les glandes surrénales est régulée par trois facteurs : l’ACTH hypophysaire, la concentration d’ions potassium dans le sang et le système angiotensine-rénine-aldostérone. En cas d’hypotension artérielle, la sécrétion d’aldostérone induite entraîne une élimination d’ions potassium et le retour à la normale de la pression artérielle.
Pensée du jour
« Hormones de jouvence ou du stress, cycle circadien, anti-inflammatoires… les corticoïdes ont toutes les vertus, mais quelques défauts ! »
Sources
– Robert Morfin, Les stéroïdes naturels de A à Z, {Editons Tec&Doc, Lavoisier, 2011
– http://en.wikipedia.org/wiki/Corticosteroid
– http://fr.wikipedia.org/wiki/Cortisol
– http://fr.wikipedia.org/wiki/Glucocorticoïde
– http://en.wikipedia.org/wiki/Mineralocorticoid
– La Chimie et le sport, EDP Sciences et {L’Actualité Chimique Livres, 2011
– www.medecine-et-sante.com/maladiesexplications/effetscortisolcortisone.html
– http://fr.wikipedia.org/wiki/Hormone_adrénocorticotrope
– http://fr.wikipedia.org/wiki/Epiandrostérone
– http://fr.wikipedia.org/wiki/Pro-opiomélanocortine
– http://fr.wikipedia.org/wiki/Syndrome_de_Cushing
– http://orthopedie.wordpress.com/la-cortisone-les-anti-inflammatoires-les-infiltrations/
– www.comite-olympique.asso.fr/files/File/actions/sante/documentation/2006/les_dangers_des_corticoides.pdf
– www.infirmiers.com/pdf/cours-en-vrac/SI-personne-sous-corticoides.pdf
– www.scribd.com/doc/23463404/Corticosteroid-Injections-and-Synoviortheses-of-the-Foot-and-Ankle-in-Rheumatoid-Arthritis
– J.L. Hollander, E.M. Brown, R.A. Jessar RA, Hydrocortisone and cortisone injected into arthritic joints, J. Am. Med. Assoc. 1951,147,1929-35
Pour en savoir plus
– Cholestérol
– Squalène
– Triterpènes polycliques
– ATP, ADP
– Morphine
– Chocolat
– Adrénaline
– ADN
– Prozac
– GAGs I
– GAGs II

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie