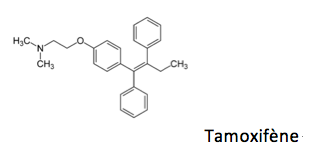
Le médicament le plus utilisé depuis une trentaine d’années est le tamoxifène, un analogue de stéroïde, qui agit sur les œstrogènes déjà formés. Son métabolite principal, actif, le 4-hydroxy-tamoxifène, est produit par un cytochrome P450 (cf. Cytochrome P450), ce qui fait que tout inhibiteur de ce cytochrome diminue l’activité du médicament…
…et peut être responsable de récidives : les interactions avec une grande variété de médicaments sont particulièrement néfastes (cis-Platine, certains antidépresseurs…).
Intervenir en amont, sur la formation même des œstrogènes, responsables du développement de ces cancers hormono-dépendants, en empêchant l’aromatisation des androgènes précurseurs, est une voie expérimentée depuis quelques années. En effet, si la source principale d’œstrogènes chez la femme non ménopausée se trouve dans les ovaires, chez la femme ménopausée, ils sont essentiellement locaux et résultent de l’action d’une enzyme, l’aromatase, concentrée dans les tissus périphériques comme les tissus adipeux, notamment du sein.
L’aromatase fait partie de la superfamille des cytochromes P450 ; elle est codée par le gène CYP19, et elle est la source œstrogénique majeure en post-ménopause, lorsque les glandes surrénales n’en produisent plus.
Conversion testostérone en œstradiol
Son activité est régulée par des promoteurs spécifiques aux tissus, qui sont à leur tour contrôlés par des hormones et d’autres facteurs. Les facteurs augmentant l’activité de l’aromatase, et donc favorisant le cancer hormono-dépendant, sont l’âge, l’obésité, l’insuline, les gonadotropines et l’alcool. L’activité de l’aromatase est diminuée par la prolactine, les hormones antimullériennes et la consommation de tabac. L’activité de l’aromatase est améliorée au niveau de certains tissus dépendants aux œstrogènes, comme ceux proches des tissus du sein, du cancer de l’endomètre, de l’endométriose et du léiomyome utérin. Par la voie aromatase, même après la ménopause, les cancers eœstrogèno-dépendants restent donc soumis à une influence hormonale d’où l’intérêt des inhibiteurs de ces aromatisations. Ils agissent au niveau de la glande mammaire mais diminuent également les œstrogènes circulants, donc les risques invasifs et de récurrence.
Ces inhibiteurs forment une classe thérapeutique récente apportant une «chimiothérapie hormonale» du cancer du sein de la femme ménopausée. Ces nouvelles molécules sont au nombre de trois, dont deux ne sont pas des stéroïdes, comme l’anastrazole et le letrozole. Généralement très spécifiques, ils sont indiqués dans les cancers du sein au stade avancé ou métastasés résistant ou en rechute après thérapeutique anti-œstrogénique classique (tamoxifène ou autre). Ils sont strictement réservés aux femmes ne risquant pas de grossesse, car ils sont peut-être tératogènes.
Letrozole et Anastrazole agissent via un couplage compétitif et réversible avec l’hème du cytochrome P450 de l’aromatase, et son action est réellement spécifique, c’est-à-dire qu’ils ne réduisent pas la production de minéralo- ou corticostéroides.
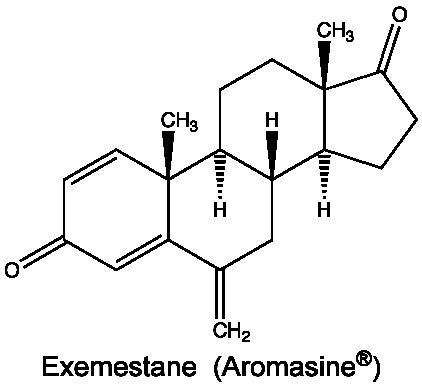
La nouveauté et l’intérêt de l’Aromasine® vient de ce que son couplage avec l’hème est irréversible. Ce stéroïde est donc un leurre « réaliste » qui inhibe l’enzyme, et constitue ce qu’on appelle un inhibiteur suicide, efficace à 85 %. L’étude MP3, présentée samedi 4 juin 2011 au colloque annuel de la société américaine de cancérologie par Paul E . Goss a permis de montrer, sur 4 560 femmes ménopausées et à risque, aux États-Unis, au Canada et en France, entre 2004 et 2010, une réduction de 65 % du risque de cancer du sein.
En outre, chez celles ayant pris de l’Aromasine®, mais ayant eu un cancer du sein ou une récurrence de la maladie lors de l’essai clinique « un grand nombre de tumeurs sont de petites tailles et il semble également y avoir moins de cancers les plus agressifs ».
L’équipe de la Harvard Medical School annonce, de plus, des effets secondaires limités dans leur nombre et leur gravité. Ils existent malgré tout (fatigue, bouffées de chaleur, insomnies, douleurs articulaires parfois violentes…), et le traitement médicamenteux doit faire l’objet d’un suivi rigoureux. Notamment, certains médicaments sont incompatibles, comme l’antibiotique rifampicine, ou des anticonvulsants utilisés dans le traitement de l’épilepsie. Les produits naturels, comme les préparations à base de millepertuis (Antihypericum perforatum), sont également à éviter…
Traitement du cancer du sein invasif, œstrogène-dépendant chez la femme ménopausée, la chimiothérapie hormonale semble donc moins toxique avec moins d’intolérance et moins d’effets secondaires que la chimiothérapie cytotoxique classique.
Pensée du jour
Chimie, chimie, en toi notre espoir quand rien ne marche plus !
Sources
– http://en.wikipedia.org/wiki/Exemestane
– http://monographs.iarc.fr/archive/
– http://fr.wikipedia.org/wiki/Tamoxifene
– www.medicinet.com/exemestane-oral/page3.htm
– www.steroid.com/Aromasin.php
– www.gyneweb.fr/Sources/revues/referenc/V1N4/TAMOXI~1.html
– http://fr.wikipedia.org/wiki/Aromatase
– http://en.wikipedia.org/wiki/Aromatase_inhibitor
– www.breastcancer.org/treatment/hormonal/aromatase_inhibitors/index.jsp
– www.france24.com/en/20110605-progress-fight-against-cancer-ovaries-breasts#
– http:/en.wikipedia.org/wiki/Letrozole
– http:/en.wikipedia.org/wiki/Anastrazole
Pour en savoir plus
– Cytochrome P 450

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie 

