L’expédition scientifique envoyée au Pérou par l’Académie Royale au milieu du XVIIIe siècle, avec le géographe Charles Marie de la Condamine et le médecin Joseph de Jussieu, put présenter, malgré quelques déboires, vols, naufrages, etc., une communication « sur l’arbre du quinquina ».

Ce fut le cas de plusieurs entrepreneurs allemands qui se lancèrent dans l’extraction à grande échelle de la quinine, marquant ainsi les débuts de leur grande industrie pharmaceutique. Aux États-Unis, un usage commercial de l’invention débuta dès 1826.
La grande aventure de la synthèse de la quinine (16 stéréoisomères) commencera peu après, avec quelques aléas et des découvertes inattendues, ce qu’on nomme « sérendipité ».
En 1856, William Henry Perkin, alors âgé de 18 ans, cherche une forme synthétique de la quinine dans le but de trouver une substance anti-malaria. Au cours de ses essais, il oxyde l’aniline par le dichromate de potassium, mais oxyde simultanément les impuretés de toluidine présentes dans le mélange produisant un solide noir, dont il tirera une solution alcoolique violette. Perkin brevète sa découverte, et commercialise la mauvéine qu’il fait fabriquer dans la première usine de colorants de synthèse à avoir jamais existé (cf. Colorants alimentaires). Le processus inverse est à l’origine de la découverte des sulfamides lors de la recherche de colorant de synthèse (cf. Sulfamides).
Ce ne sera qu’en 1918, qu’une première synthèse partielle sera publiée par Paul Rabe et Karl Kindler, permettant de passer de la quinotoxine à la quinine en 3 étapes.
L’occupation japonaise des zones de production de l’écorce de quinquina, et le besoin pressant d’anti-paludéens pour les soldats alliés, stimulèrent la recherche de voies de synthèse. En 1944, Robert Burns Woodward et William von Eggers Doering publieront la première synthèse totale en 17 étapes … de la D-quinotoxine, considérant que la suite du travail était connue. A la même époque, Gilbert Stork (joliment appelé Cigogne de Gilbert dans certaines traductions), avait lui aussi commencé une approche, très différente, de la synthèse totale de la quinine, à partir de (S)-4-vinylbutyrolactone, qu’il publiera en 2001.
Profitant de l’occasion, il expliquera que celle-ci n’avait jamais été synthétisée en 1944, et que si Woodward et Doering avaient tenté de reproduire les trois dernières étapes, ils auraient certainement échoué, sous-entendant qu’ils l’avaient peut-être fait… En février 2008, deux chimistes de Colorado State University, Aaron Smith et Robert Williams, rendront justice et à Rabe et Kindler et à Woodward et von Doering, en montrant que l’étape finale de réduction de la quininone en quinine, si elle est infructueuse avec l’aluminium, est très efficace avec de la poudre mal conservée et oxydée, ce qui dût être le cas en 1918 !
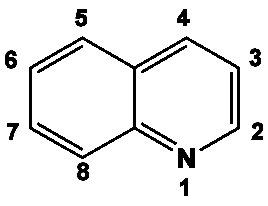
Les APS comprennent principalement les amino-8 quinoléines (primaquine, non disponible en France), la mépacrine (ou quinacrine) qui a été retirée du marché du fait d’un spectre antipaludéen incomplet et de l’importance de ses effets secondaires, les amino-4 quinoléines (les plus utilisés étant la chloroquine, synthétisée à partir de la mépacrine, l’hydroxychloroquine, dérivée de la chloroquine par β-hydroxylation et l’amodiaquine, disponible sous forme de chlorhydrate). L’accumulation tissulaire, notamment oculaire, limite l’utilisation de ces antipaludéens pourtant à large spectre et très efficaces, d’autant qu’ils induisent à terme des phénomènes de résistance.
En l’absence de vaccin, pourtant objet d’une recherche active, d’autres molécules peu onéreuses ont donc été et sont étudiées, étant donné les terribles ravages de la malaria, surtout depuis l’interdiction du DDT (cf. DDT), décision questionnée dans un tout récent article. Il s’agit soit de pharmacopée traditionnelle, comme dans le cas de l’artémisine (qing hao su, 青蒿素, en chinois), un alcaloïde extrait de l’armoise annuelle, soit d’autres molécules « naturelles » comme l’ivermectine, isolée de la bactérie {Streptomyces avermitilis en cours d’expérimentation en Afrique Noire (les avermectines sont cependant des neurotoxiques redoutables). Il peut s’agir de molécules d’une grande originalité, comme la molécule hybride, possédant deux pharmacophores, conçue par Bernard Meunier, en s’appuyant sur la connaissance de la vie du parasite et le mécanisme d’action de l’artémisine.
Espérant éviter, ou même simplement ralentir, le phénomène de résistance, l’OMS a préconisé l’utilisation de mélanges, artémisine et méfloquine (Lariam®) ou chloroquine dans une infusion de trois plantes du genre botanique Strychnos (une vaste famille dont seuls sept représentants contiennent de la strychnine) (cf. Strychnine). Toxicomanes, attention cependant aux compositions originales, fussent-elles d’origine entièrement naturelle : la quinine, mélangée à l’ergotamine, donne une poudre qui a l’aspect et le goût de l’héroïne mais provoque une mort instantanée.
Pensée du jour
« Exploiter intelligemment l’imprévu, c’est s’ouvrir sur l’avenir ; mais expérimenter n’importe quoi, n’importe comment, ce n’est pas de la sérendipité ! »
Sources
– http://fr.wikipedia.org/wiki/Quinquina
– http://fr.wikipedia.org/wiki/Quinine
– http://fr.wikipedia.org/wiki/Sérendipité
– www.repere-medical.com/article-232.html
– www.larecherche.fr/content/recherche/article?id=22988
– www.rsc.org/chemistryworld/News/2008/February/05020801.asp
– http://fr.wikipedia.org/wiki/Quinoléine
– http://fr.wikipedia.org/wiki/Quinacrine
– Bouwman H., van den Berg H. et Kylin H., DDT and Malaria Prevention : Adressing the Paradox, Environmental Health Perspectives, 2011, 119(6), 744-745.
– http://fr.wikipedia.org/wiki/Artemisia_annua
– http://fr.wikipedia.org/wiki/Artémisinine
– http://fr.wikipedia.org/wiki/Ivermectine
– La Chimie et la Santé, EDP Sciences et L’Actualité Chimique Livres, 2010
– Le magasin du Bon Dieu, Pierre Potier, JC Lattès Ed. 2001
Pour en savoir plus
– Chocolat
– Colorants alimentaires
– Sulfamides
– DDT
– Strychnine

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie 

