Selon Pline l’Ancien (Naturalis Historica, 77), les premiers hommes à produire du verre furent des marins phéniciens. Ces derniers voulurent établir leur camp sur une plage près du fleuve Belus en Asie Mineure et ne pouvant trouver de pierres pour constituer leur foyer, utilisèrent des blocs de natron (cf. Carbonate de sodium) qu’ils transportaient dans leur navire. Avec la chaleur du feu, le sable et la soude se transformèrent en pâte de verre. Pour Christopher Merrett (L’Art du Verre, 1662), « il est bien difficile lorsqu’on a mis le feu à un fourneau à brique ou en pots, qu’il n’y en ait pas une partie qui tourne en verre ; c’est pourquoi je ne balancerais pas à faire remonter son origine jusqu’au temps de la Tour de Babel ».
Si le verre fut d’abord employé pour créer des glaçures à la surface de pièces en céramique (cf. Émail), les premiers objets en verre jamais trouvés, sont des perles de verre égyptiennes remontant à 2 500 avant notre ère. On a également trouvé en Mésopotamie des baguettes de verre qui pourraient bien être plus anciennes encore. Les premiers objets à vocation utilitaire sont à mettre au crédit des Egyptiens : il s’agit de petites bouteilles et de gobelets. C’était des objets moulés.
Le soufflage du verre a été inventé par les Babyloniens vers 250 avant J.-C., rendant facile et bon marché la réalisation de vaisselle en verre. Cette technique qui évolua peu jusqu’au XVIIIe siècle consiste à recueillir la matière vitreuse en fusion (la paraison) au bout d’une tige métallique creuse, la canne à souffler. L’artisan peut alors faire rouler la bulle de verre sur la table de travail (le marbre) afin de lui donner une forme symétrique.
Les Romains firent venir des souffleurs de verre syriens et babyloniens et développèrent l’industrie des bols et des petites bouteilles en verre.
L’effondrement de l’Empire romain arrêta le développement des technologies du verre qui disparut progressivement d’Europe. À l’exception des vitraux des cathédrales gothiques, il a fallu attendre leur renaissance à Venise au XIIIe et XIVe siècle grâce aux contacts que les Vénitiens entretenaient avec les Byzantins qui avaient su préserver ce savoir-faire. Le cristallo se répandit rapidement au-delà des Alpes et en Angleterre où le verre au plomb de Stephen Falango remplaça le fragile cristallo.
Ce n’est qu’au XVIIe siècle que Colbert, las de voir sortir de France des sommes considérables pour l’importation de miroirs de Venise, fit porter son effort sur le verre plat. La Manufacture Royale des Glaces et la mise au point du procédé de coulée par Louis-Lucas de Néhou affranchirent totalement la France des procédés vénitiens. Le verre fut également poncé et poli ce qui le rendait désormais complètement transparent.
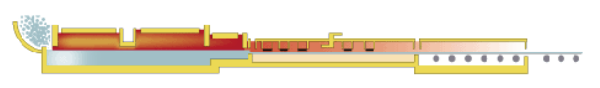
Au XIXe siècle, la technologie du verre plat s’améliora conduisant à la fabrication de grandes plaques de verre. La France, la Belgique et l’Allemagne monopolisèrent la fabrication de plaques de verre jusqu’à la création en 1833 de la première usine américaine avec la Pittsburgh Plate Glass Co., plus connu sous le sigle PPG. En France se constituent deux groupes verriers, l’un autour de Saint-Gobain, héritier de la Manufacture royale des glaces, l’autre de Boussois devenue un temps BSN. Le XXesiècle accentua la mécanisation avec la production de rubans de verre sans fin, simultanément polis des deux côtés et l’invention du procédé float glass par Pilkington qui changea la face de l’industrie du verre plat.
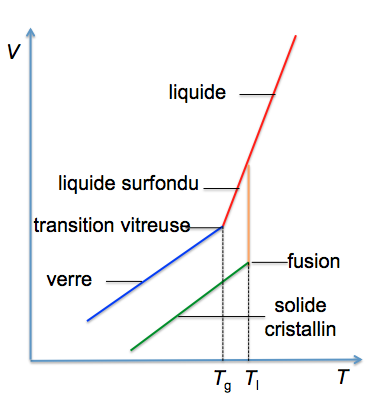
Selon Jerzy Zaraycki, le verre est un « solide non cristallin présentant le phénomène de transition vitreuse ». Encore faut-il définir ce qu’est cette transition! Dans le cas d’un liquide suffisamment visqueux à la température de fusion (Tl) pour permettre la formation d’un liquide en surfusion, le volume de ce liquide se place d’abord dans l’extrapolation de l’évolution du volume au-dessus de Tl, mais à une température Tg où la viscosité devient très élevée, il y a changement de pente signalant la transition vitreuse.
En-dessous de Tg, la variation de volume avec la température est similaire à celle du solide cristallin. Par contre, à Tg, il n’y a pas de changement de volume, contrairement à ce qui se produit le plus souvent lorsqu’il y a conversion d’un liquide en solide cristallin. La structure en-dessous de Tg resterait donc similaire au liquide surfondu qui est celle du liquide : c’est la caractéristique d’un verre, matériau qui a la structure d’un liquide, mais les propriétés d’un solide. La transition vitreuse se manifeste également lorsqu’un verre est réchauffé. Ce phénomène permet de distinguer le verre d’autres solides amorphes.
La structure d’un verre est telle qu’il n’existe aucun ordre à grande distance. Un verre peut même être vu comme un « réseau » tridimensionnel, semblable à celui d’un cristal, mais dans lequel seul l’ordre à courte distance est conservé. Ainsi la structure de la silice cristalline (cristobalite) est constituée par l’agencement ordonné de tétraèdres SiO4, alors que celle de la silice vitreuse correspond à un empilement anarchique de ces mêmes tétraèdres, comme le montrent schématiquement les représentations bidimensionnelles :
– Un verre est traditionnellement composé :
– d’un formateur de réseau qui est la silice (ou sable très pur), SiO2, le bore sous sa forme oxyde B2O3 (cf. Bore), le phosphore sous sa forme oxyde P2O5 (cf. Phosphore), le germanium sous sa forme oxyde GeO2 (cf. Germanium) et l’arsenic sous sa forme oxyde As2O3 (cf. Arsenic),
– d’un fondant qui abaisse la température de fusion, mais aussi la viscosité : c’est souvent un oxyde alcalin Na2O (cf. Sodium) ou K2O (cf. Potassium) capable de rompre les ponts oxygène reliant les tétraèdres SiO4 du réseau vitreux, provoquant une dépolymérisation de ce dernier. Ils transforment alors les oxygènes pontants, qui lient deux éléments formateurs de réseau, en oxygènes non-pontants, liés à un seul formateur de réseau,
– d’un modificateur de type métallique tel, MgO, Al2O3, CaO, PbO ou B2O3, voire des éléments de transition ou des lanthanides.
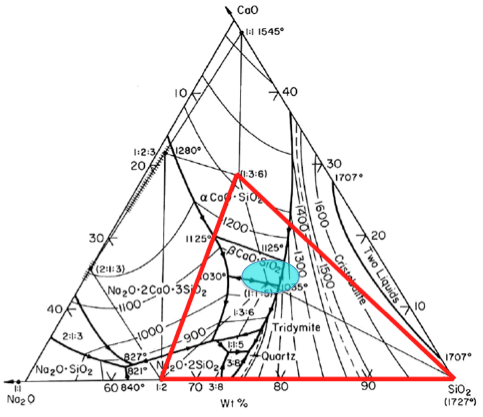
L’addition de chaux, CaO (cf. Chaux), renforce la stabilité des verres sodés qui sont attaqués par l’eau. L’examen du diagramme de phase ternaire SiO2-Na2O-CaO montre la complexité du système où la zone des verres industriels figure essentiellement dans l’ovale bleu clair.
Cette complexité est encore renforcée par le fait que l’addition d’autre adjuvants (magnésie, cf. Magnésium, alumine, cf. Aluminium, etc.) améliorent les propriétés mécaniques de ces matériaux aux températures d’élaboration du liquide et de ses propriétés rhéolgiques, puis des techniques de mise en œuvre (étirage, etc.) pour l’obtention des variétés requises.
Une variété chère au chimiste est celle incorporant l’oxyde B2O3, découverte en 1887 par l’allemand Otto Schott et développée par la suite par Corning sous la marque Pyrex. Les verres sodocalciques représentent 90 % de la production totale de verres.
Le verre est un matériau de construction très important dans l’architecture moderne et dans l’industrie automobile. Il est également présent sous forme de laine de verre, isolant léger, imputrescible et ininflammable et la brique de verre est utilisée pour réaliser des parois translucides.
Il est également utilisé dans l’industrie agroalimentaire : réagissant très peu avec la plupart des produits utilisés dans ce domaine, c’est un matériau idéal pour les contenants (bouteilles, pots de yaourt, et autres emballages). Du fait de sa structure désordonnée, c’est le matériau dans lequel sont confinés par le procédé de vitrification les déchets radioactifs de haute activité, car il permet d’absorber sans trop de dommages structuraux une partie des radiations.
Le verre est utilisé en optique essentiellement pour ses propriétés réfringentes (lentilles, verres de lunettes) et, enfin, les utilisations artistiques du verre sont innombrables depuis les origines, qui font aussi appel à de nombreuses innovations techniques.
Bref, et c’est la
Pensée du jour
« Envers et contre tout, c’est en verre et pour tout ! »
Pour en savoir plus
– P. Richet, {L’âge du verre, Gallimard, 2000 (ISBN : 2-07-053518-5).
– La Chimie et l’Art, EDP Sciences & L’Actualité Chimique Livres, 2010 (ISBN : 978-2-7598-0527-3).
– http://fr.wikipedia.org/wiki/Verre
– http://www.verreonline.fr/
– http://universduverre.free.fr/dossiers/verre-float.html
– http://universduverre.free.fr/dossiers/verre-trempe.htm
– http://en.wikipedia.org/wiki/Glass
Pour en savoir plus
– Émail
– Verres intelligents
– Carbonate de sodium
– Bore
– Phosphore
– Germanium
– Arsenic
– Sodium
– Potassium
– Chaux
– Magnésium
– Aluminium

 Présentation
Présentation  Entités
Entités  Partenaires
Partenaires  Histoire de la SCF
Histoire de la SCF  Gouvernance
Gouvernance  Industrie
Industrie